Có một hh gồm Al2O3; Fe2O3 ; CaCO3 trong đó Al2O3 chiếm 10,2% ; Fe2O3 chiếm 9,8%.Đem nung hh ở nhiệt độ cao thu đc chất rẳn có khối lượng 67% khối lượng hh ban đầu. Tính khối lượng các chất trong chất rắn thu đc

Những câu hỏi liên quan
Hóa Học · Lớp 8Có một hh gồm CaCO3, MgCO3 và Al2O3 trong đó khối lượng Al2O3 nặng bằng 1/8 khối lượng muối cacbonat. Đem nung nóng hh đến khi hh bị phân hủy hoàn toàn ta thu được chất rắn có khối lượng bằng 6/10 khối lượng của hh ban đầu. a) Viết PTHH b) Tính thành phần % về khối lượng của MgCO3 trong hh ban đầu?mn nhanh một chút ,mik đang cần gấp
Đọc tiếp
Hóa Học · Lớp 8
Có một hh gồm CaCO3, MgCO3 và Al2O3 trong đó khối lượng Al2O3 nặng bằng 1/8 khối lượng muối cacbonat. Đem nung nóng hh đến khi hh bị phân hủy hoàn toàn ta thu được chất rắn có khối lượng bằng 6/10 khối lượng của hh ban đầu. a) Viết PTHH b) Tính thành phần % về khối lượng của MgCO3 trong hh ban đầu?
mn nhanh một chút ,mik đang cần gấp
Gọi KL của Al2O3 là x g thì KL muối Cacbonat là 8x g
=> KL hỗn hợp là 9x g
Do sau phân hủy thì khối lượng còn 6/10 ban đầu
=> KL CO2 bay đi là \(9x\left(1-\dfrac{6}{10}\right)=3,6x\)
Khi đó số mol muối cacbonat = số mol của CO2 = \(\dfrac{3,6x}{44}\)
Giờ ta giả sử cho dễ tính toán nha, để số tròn thì mình lấy x=11
Tổng khối lượng muối cacbonat là 88g => 100a + 84b = 88 (1)
Tổng số mol muối cacbonat là 0,9 mol => a + b = 0,9 (2)
Từ (1) và (2) ta có => a = 0,775 mol; b = 0,125 mol
=> %KL MgCO3 = \(\dfrac{\left(84x0,125\right)x100\%}{99}=10,6\%\)
Đúng 0
Bình luận (0)
a)
$CaCO_3 \xrightarrow{t^o} CaO + CO_2$
$MgCO_3 \xrightarrow{t^o} MgO + CO_2$
b)
Coi m hh = 102(gam)
Suy ra : m Al2O3 = 102/8 = 12,75(gam)
Gọi n CaCO3 = a(mol) ; n MgCO3 = b(mol)
=> 100a + 84b + 12,75 = 102(1)
m hh sau = 102.6/10 = 61,2(gam)
Bảo toàn khối lượng :
m CO2 = 102 -61,2 = 40,8(gam)
=> a + b = 40,8/44 = (2)
Từ (1)(2) suy ra a = 0,71 ; b = 153/704
Suy ra :
m MgCO3 = 153/704 .84 = 18,25(gam)
%m MgCO3 = 18,25/102 .100% = 17,9%
Đúng 2
Bình luận (1)
Một loại đá vôi có chứa 80% CaCO3, 10,2% Al2O3 và 9,8% Fe2O3 về khối lượng. Nung đá ở nhiệt độ cao ta thu được chất rắng có khối lượng bằng 73,6% khối lượng đá trước khi nung. Hiệu suất của quá trình phân hủy CaCO3 là: A. 37,5% B. 75% C. 62,5% D. 8,25%
Đọc tiếp
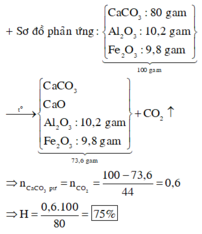
Một loại đá vôi có chứa 80% CaCO3, 10,2% Al2O3 và 9,8% Fe2O3 về khối lượng. Nung đá ở nhiệt độ cao ta thu được chất rắng có khối lượng bằng 73,6% khối lượng đá trước khi nung. Hiệu suất của quá trình phân hủy CaCO3 là:
A. 37,5%
B. 75%
C. 62,5%
D. 8,25%
Đáp án : B
Giả sử khối lượng đá vôi là 100g
=> mCaCO3 = 80g => nCaCO3 = 0,8 mol
=> msau = 73,6g => mtrước – msau = 100 – 73,6 = mCO2
=> nCO2 = nCaCO3 pứ = 0,6 mol
=> H%pứ = 75%
Đúng 0
Bình luận (0)
Một loại đá vôi có chứa 80% CaCO3, 10,2% Al2O3 và 9,8% Fe2O3 về khối lượng. Nung đá ở nhiệt độ cao, thu được chất rắn có khối lượng bằng 73,6% khối lượng đá trước khi nung. Hiệu suất của quá trình phân hủy CaCO3 là A. 37,5%. B. 75%. C. 62,5%. D. 8,25%.
Đọc tiếp
Một loại đá vôi có chứa 80% CaCO3, 10,2% Al2O3 và 9,8% Fe2O3 về khối lượng. Nung đá ở nhiệt độ cao, thu được chất rắn có khối lượng bằng 73,6% khối lượng đá trước khi nung. Hiệu suất của quá trình phân hủy CaCO3 là
A. 37,5%.
B. 75%.
C. 62,5%.
D. 8,25%.
1) có 3 dung dịch H2SO4: dung dịch A có nồng độ 14,3M ( D1,43 g/ml). dung dịch B có nồng độ 2,18M ( D1,09 g/ml). dung dịch C có nồng độ 6,1M( D 1,22 g/ml). trộn A vs B theo tỉ lệ:
a) thể tích bằng bao nhiêu để thu được dung dịch C.
b) tỉ lệ khối lượng dung dịch bằng bao nhiêu để thu được dung dịch C.
2) hỗn hợp gồm CaCO3 có lẫn Al2O3 và Fe2O3 trong đó Al2O3 chiếm 10,2%, Fe2O3 chiếm 9,8%. nung hỗn hợp ở nhiệt độ cao thu được chất rắn có khối lượng 67% khối lượng hỗn hợp ban đầu. tính phần trăm...
Đọc tiếp
1) có 3 dung dịch H2SO4: dung dịch A có nồng độ 14,3M ( D=1,43 g/ml). dung dịch B có nồng độ 2,18M ( D=1,09 g/ml). dung dịch C có nồng độ 6,1M( D= 1,22 g/ml). trộn A vs B theo tỉ lệ:
a) thể tích bằng bao nhiêu để thu được dung dịch C.
b) tỉ lệ khối lượng dung dịch bằng bao nhiêu để thu được dung dịch C.
2) hỗn hợp gồm CaCO3 có lẫn Al2O3 và Fe2O3 trong đó Al2O3 chiếm 10,2%, Fe2O3 chiếm 9,8%. nung hỗn hợp ở nhiệt độ cao thu được chất rắn có khối lượng 67% khối lượng hỗn hợp ban đầu. tính phần trăm khối lượng các chất rắn thu được sau khi nung.
b) Đưa khối lượng hỗn hợp về 100g thì ta có khối lượng chất rắn sau pư là 67g.
mAl2O3=\(\dfrac{100}{100}\cdot10,2\) =10.2 g
mFe2O3=\(\dfrac{100}{100}\cdot9,8\) =9,8 g
mCaCO3= 100-(10.2+9.8)=80g
PTHH: CaCO3 ----t0--> CaO+ CO2
1 1 1
Khối lượng chất rắn hao hụt sau pư là khối lượng CO2.
mCO2=100-67=33g
=>nCO2= 33/44=0.75 mol
mCaCO3=0.75*100=75g
mCaCO3 dư= 80-75=5g
mCaO=0.75*56=42g
%CaCO3=5/67*100=7.46%
%CaO=42/67*100=62.7%
%Al2O3=10.2/67*100=15.2%
=>%Fe2O3=14.64%
Đúng 0
Bình luận (0)
Bài 1 : Khử hoàn toàn 20g hh A gồm Fe2O3 vá CuO khí H2 ở nhiệt độ cao thu đc hh kim loại và hơi nước . Biết Fe2O3 chiếm 80% khối lượng hh A a, Viết các PTHH b, Tính thể tích H2 ( đktc ) đã dùng c, Tính khối lượng hh B thu đc Bài 2 : Cho hh X gồm CuO và Fe2O3 tác dụng với khí H2 ở nhiệt độ cao thu đc 26,4g hh kim loại Y trong đó khối lượng Cu gấp 1,2 lần khối lượng Fe.a, Tính thể tích H2 ( đktc ) cần dùng .b, Tính khối lượng hh X và thành phần % theo khối lượng các chất trong X Bài 3 : Dùng khí...
Đọc tiếp
Bài 1 : Khử hoàn toàn 20g hh A gồm Fe2O3 vá CuO = khí H2 ở nhiệt độ cao thu đc hh kim loại và hơi nước . Biết Fe2O3 chiếm 80% khối lượng hh A
a, Viết các PTHH
b, Tính thể tích H2 ( đktc ) đã dùng
c, Tính khối lượng hh B thu đc
Bài 2 : Cho hh X gồm CuO và Fe2O3 tác dụng với khí H2 ở nhiệt độ cao thu đc 26,4g hh kim loại Y trong đó khối lượng Cu gấp 1,2 lần khối lượng Fe.
a, Tính thể tích H2 ( đktc ) cần dùng .
b, Tính khối lượng hh X và thành phần % theo khối lượng các chất trong X
Bài 3 : Dùng khí CO để khử hoàn toàn 31,2g hh gồm CuO và Fe3O4 , trong hh này khối lượng Fe3O4 nhiều hơn khối lượng CuO là 15,2g
a, Tính khối lượng các kim loại thu đc
b, Tính thể tích CO đã phản ứng và thể tích CO2 thu đc ( đktc )
Mong các cao nhân giúp em gấp , 2 hôm nữa em phải nộp bài :(
Bài 1:
a) PTHH: \(Fe_2O_3+3H_2\xrightarrow[]{t^o}2Fe+2H_2O\)
\(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
b) Ta có: \(\left\{{}\begin{matrix}m_{Fe_2O_3}=20\cdot80\%=16\left(g\right)\\m_{CuO}=20-16=4\left(g\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\\n_{CuO}=\dfrac{4}{80}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{H_2}=3n_{Fe_2O_3}+n_{CuO}=0,35\left(mol\right)\) \(\Rightarrow V_{H_2}=0,35\cdot22,4=7,84\left(l\right)\)
c) Theo các PTHH: \(\left\{{}\begin{matrix}n_{Fe}=2n_{Fe_2O_3}=0,2\left(mol\right)\\n_{Cu}=n_{CuO}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{hhB}=m_{Fe}+m_{Cu}=0,2\cdot56+0,05\cdot64=14,4\left(g\right)\)
Đúng 3
Bình luận (4)
Bài 2:
PTHH: \(Fe_2O_3+3H_2\xrightarrow[]{t^o}2Fe+3H_2O\)
\(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
a) Vì khối lượng Cu bằng \(\dfrac{6}{5}\) khối lượng Fe
\(\Rightarrow\left\{{}\begin{matrix}m_{Cu}=\dfrac{26,4}{6+5}\cdot6=14,4\left(g\right)\\m_{Fe}=26,4-14,4=12\left(g\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{Cu}=\dfrac{14,4}{64}=0,225\left(mol\right)\\n_{Fe}=\dfrac{12}{56}=\dfrac{3}{14}\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{H_2}=\dfrac{3}{2}n_{Fe}+n_{Cu}=\dfrac{9}{28}+0,225=\dfrac{153}{280}\left(mol\right)\) \(\Rightarrow V_{H_2}=\dfrac{153}{280}\cdot22,4=12,24\left(l\right)\)
b) Theo các PTHH: \(\left\{{}\begin{matrix}n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=\dfrac{3}{28}\left(mol\right)\\n_{CuO}=n_{Cu}=0,225\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe_2O_3}=\dfrac{3}{28}\cdot160\approx17,14\left(g\right)\\m_{CuO}=0,225\cdot80=18\left(g\right)\end{matrix}\right.\) \(\Rightarrow m_{hh}=35,14\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe_2O_3}=\dfrac{17,14}{35,14}\cdot100\%\approx48,78\%\\\%m_{CuO}=51,22\%\end{matrix}\right.\)
Đúng 2
Bình luận (2)
Bài 3:
PTHH: \(CuO+CO\xrightarrow[]{t^o}Cu+CO_2\uparrow\)
\(Fe_3O_4+4CO\xrightarrow[]{t^o}3Fe+4CO_2\uparrow\)
a) Ta có: \(\left\{{}\begin{matrix}m_{Fe_3O_4}=\dfrac{31,2+15,2}{2}=23,2\left(g\right)\\m_{CuO}=31,2-23,2=8\left(g\right)\end{matrix}\right.\)
\(\Rightarrow n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)=\dfrac{8}{80}=n_{CuO}\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,3\left(mol\right)\\n_{Cu}=0,1\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,3\cdot56=16,8\left(g\right)\\m_{Cu}=0,1\cdot64=6,4\left(g\right)\end{matrix}\right.\)
b) Theo các PTHH: \(n_{CO}=n_{CO_2}=n_{Cu}+\dfrac{4}{3}n_{Fe}=\dfrac{7}{30}\left(mol\right)\)
\(\Rightarrow V_{CO}=V_{CO_2}=\dfrac{7}{30}\cdot22,4\approx5,23\left(l\right)\)
Đúng 2
Bình luận (0)
Bài 3: Nung 2,22g hh X gồm Al2O3, MgO, Fe2O3 trong dòng khí CO dư đến pư hoàn toàn, thu được chất rắn Y có khối lượng 1,98 g. Để hòa hết lượng Y trên cần 100ml dd HCl 1M. Tính % khối lượng mỗi chất trong hh X.
Đặt \(\left\{{}\begin{matrix}n_{Al_2O_3}=a\left(mol\right)\\n_{MgO}=b\left(mol\right)\\n_{Fe_2O_3}=c\left(mol\right)\end{matrix}\right.\) \(\Rightarrow102a+40b+160c=2,22\)
\(Al_2O_3,MgO\) không bị khử bởi \(CO\)
\(PTHH:Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
\(\left(mol\right)\) \(c\) \(2c\)
\(\Rightarrow102a+40b+56.2c=1,98\)
\(PTHH:Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
\(\left(mol\right)\) \(a\) \(6a\)
\(PTHH:MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(\left(mol\right)\) \(b\) \(2b\)
\(PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\)
\(\left(mol\right)\) \(2c\) \(4c\)
\(\Rightarrow6a+2b+4c=0,1\)
Từ đó: \(\left\{{}\begin{matrix}a=0,01\left(mol\right)\\b=0,01\left(mol\right)\\c=0,005\left(mol\right)\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}\%m_{Al_2O_3}=45,95\left(\%\right)\\\%m_{MgO}=18,02\left(\%\right)\\\%m_{Fe_2O_3}=36,03\left(\%\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
3. Đặt nAl2O3= x, nMgO=y, nFe2O3 = z
PTHH:
Fe2O3 + 3CO-----> 2Fe + 3CO2
Al2O3 + 6HCl ------> 2AlCl3 + 3H2O
MgO + 2HCl --------> MgCl2 + H2O
Fe + 2HCl -------> FeCl2 + H2
Ta có khối lượng của hỗn hợp X : \(102x+40y+160z=2,22\) (1)
Chất rắn Y gồm Fe, MgO và Al2O3
=> \(56.2z+102x+40y=1,98\) (2)
Theo PT ta có : \(n_{HCl}=6x+2y+2z.2=0.1.1\) (3)
Từ (1), (2), (3) => x=0,01 ; y=0,01, z= 0,005
=> \(\%m_{Al_2O_3}=\dfrac{0,01.102}{2,22}.100=45,95\%\)
\(\%m_{MgO}=\dfrac{0,01.102}{2,22}.100=18,01\%\)
=>\(\%m_{Fe_2O_3}=\dfrac{0,005.160}{2,22}.100=36,04\%\)
Đúng 0
Bình luận (0)
hh A gồm CuO,Fe2O3,Al2O3. Để khử hết 200 g hh A cần dùng hết V lít H2(đktc), sau khi các PƯ xảy ra hoàn toàn thu được chất rắn B có khối lượng là 156 g (Biết tỉ lệ số mol giữa CuO và Fe2O3 trong hh A là 1:1,5)a, tính V ở đktcb, tính % khối lượng mỗi chất trong hh Ac, Nếu 1/5 lượng khí H2 dùng ở trên PƯ với 36 g FeO thu được 29,6 g chất rắn. Tính hiệu suất PƯ
Đọc tiếp
hh A gồm CuO,Fe2O3,Al2O3. Để khử hết 200 g hh A cần dùng hết V lít H2(đktc), sau khi các PƯ xảy ra hoàn toàn thu được chất rắn B có khối lượng là 156 g (Biết tỉ lệ số mol giữa CuO và Fe2O3 trong hh A là 1:1,5)
a, tính V ở đktc
b, tính % khối lượng mỗi chất trong hh A
c, Nếu 1/5 lượng khí H2 dùng ở trên PƯ với 36 g FeO thu được 29,6 g chất rắn. Tính hiệu suất PƯ
a) Gọi số mol H2 là x
=> \(n_{H_2O}=x\left(mol\right)\)
Theo ĐLBTKL: \(m_A+m_{H_2}=m_B+m_{H_2O}\)
=> 200 + 2x = 156 + 18x
=> x = 2,75 (mol)
=> \(V_{H_2}=2,75.22,4=61,6\left(l\right)\)
b) Gọi \(\left\{{}\begin{matrix}n_{CuO}=a\left(mol\right)\\n_{Fe_2O_3}=1,5a\left(mol\right)\\n_{Al_2O_3}=b\left(mol\right)\end{matrix}\right.\)
=> 80a + 240a + 102b = 200
=> 320a + 102b = 200
PTHH: CuO + H2 --to--> Cu + H2O
a---------------->a
Fe2O3 + 3H2 --to--> 2Fe + 3H2O
1,5a------------------>3a
=> 64a + 168a + 102b = 156
=> 232a + 102b = 156
=> a = 0,5; b = \(\dfrac{20}{51}\)
=> \(\left\{{}\begin{matrix}\%m_{CuO}=\dfrac{0,5.80}{200}.100\%=20\%\\\%m_{Fe_2O_3}=\dfrac{0,75.160}{200}.100\%=60\%\\\%m_{Al_2O_3}=\dfrac{\dfrac{20}{51}.102}{200}.100\%=20\%\end{matrix}\right.\)
c) \(n_{H_2}=\dfrac{2,75}{5}=0,55\left(mol\right)\)
\(n_{FeO\left(tt\right)}=\dfrac{36}{72}=0,5\left(mol\right)\)
Gọi số mol FeO phản ứng là t (mol)
PTHH: FeO + H2 --to--> Fe + H2O
t--------------->t
=> 56t + (0,5-t).72 = 29,6
=> t = 0,4 (mol)
=> \(H\%=\dfrac{0,4}{0,5}.100\%=80\%\)
Đúng 4
Bình luận (0)
Có một hh B gồm Al2O3 , MgCO3 , CaCO3 trong đó khối lượng Al2O3 bằng tổng khối lượng 2 muối cácbonat. Nung B đến khối lượng không đổi thì khối lượng chất rắn còn lại chỉ bằng khối lượng của B .Xác định % khối lượng mỗi chất trong B . ( 11,11%; 10,61% ;78,28% )
Đọc tiếp
Có một hh B gồm Al2O3 , MgCO3 , CaCO3 trong đó khối lượng Al2O3 bằng tổng khối lượng 2 muối cácbonat. Nung B đến khối lượng không đổi thì khối lượng chất rắn còn lại chỉ bằng
khối lượng của B .Xác định % khối lượng mỗi chất trong B . ( 11,11%; 10,61% ;78,28% )
hỗn hợp X gồm CaCO3,MgCO3 và Al2O3, trong đó khối lượng của Al2O3 bằng 1/10 khối lượng các muối cacbonat. nung X ở nhiệt độ cao đến khối lượng không đổi thu được chất rắn Y có khối lượng bằng 56,8% khối lượng hỗn hợp X. tính % khối lượng mỗi chất trong X
Gọi \(n_{CaCO_3}=x\left(mol\right);n_{MgCO_3}=y\left(mol\right)\)
\(m_{Al_2O_3}=\dfrac{100x+84y}{10}\)
Bảo toàn Ca \(\Rightarrow n_{CaO}=n_{CaCO_3}=x\left(mol\right)\)
Bảo toàn Mg \(\Rightarrow n_{MgO}=n_{MgCO_3}=y\left(mol\right)\)
\(\Rightarrow m_Y=m_{CaO}+m_{MgO}+m_{Al_2O_3}\)\(=56x+40y+\dfrac{100x+84y}{10}\)
\(\Rightarrow56x+40y+\dfrac{100x+84y}{10}=56,8\%.m_X=56,8\%.\dfrac{11}{10}.\left(100x+84y\right)\)
\(=\dfrac{781}{1250}.\left(100x+84y\right)\)\(\Leftrightarrow56x+40y=\dfrac{328}{625}\left(100x+84y\right)\)
\(\Leftrightarrow x=\dfrac{29}{25}y\)
\(\%m_{CaCO_3}=\dfrac{100x}{\dfrac{11}{10}.\left(100x+84y\right)}.100\%=\dfrac{100.\dfrac{29}{25}y}{\dfrac{11}{10}.\left(100.\dfrac{29}{25}y+84y\right)}.100\%\approx52,73\left(\%\right)\)
\(\%m_{MgCO_3}=\dfrac{84y}{\dfrac{11}{10}.\left(100x+84y\right)}.100\%=\dfrac{84y}{\dfrac{11}{10}.\left(100.\dfrac{29}{25}y+84y\right)}.100\%\approx38,18\left(\%\right)\)
\(\Rightarrow\%m_{Al_2O_3}\approx9,09\left(\%\right)\)
Đúng 1
Bình luận (0)